
東京大学 定量生命科学研究所 分子神経生物学研究分野 准教授
助成期間:令和2年度〜 キーワード:クロマチン エピジェネティクス ニューロン 研究室ホームページ
2010年3月東京大学工学系研究科化学生命工学専攻博士課程 単位取得卒業。日本学術振興会特別研究員(DC1)、東京大学分子細胞生物学研究所学術支援専門職員となり、2012年5月に学位取得(工学博士)。その後、東京大学分子細胞生物学研究所助教、同大学大学院薬学系研究科講師を経て、2022年4月より東京大学定量生命科学研究所、2023年4月より同大学大学院薬学系研究科協力講座の准教授となり、現在に至る。
生物が必要なたんぱく質を生成するためにDNAの一部をコピーすることを「転写」といいます。ただし、人間やマウスのDNAは30億塩基対あります。つまりDNAとは、30億文字の設計書のようなものです。
その中身をすべて確認するのではなく、必要な部分のみを適切に選んで転写するためには、どうしたらいいと思いますか?
付箋をつけたり、しおりを挟んでおくことです。
しおりの色によって「今から転写する部分」「転写してはいけない部分」「後で転写する部分」などを区別できるとイメージしてください。このようにDNAの転写を、DNAやタンパク質への化学修飾によって制御する仕組みを、エピジェネティクスと呼びます。
もう一つ、エピジェネティクスの重要な要素となっているのが、クロマチン構造です。
DNAはヒストンというたんぱく質に巻きついており、「DNA+ヒストン」をヌクレオソーム、ヌクレオソームが螺旋状に積み重なった状態をクロマチンと呼びます。
このクロマチンが凝集(クローズ)していると転写が発生しにくい。逆に、凝集していない(オープン)部分は転写が起こりやすくなります。
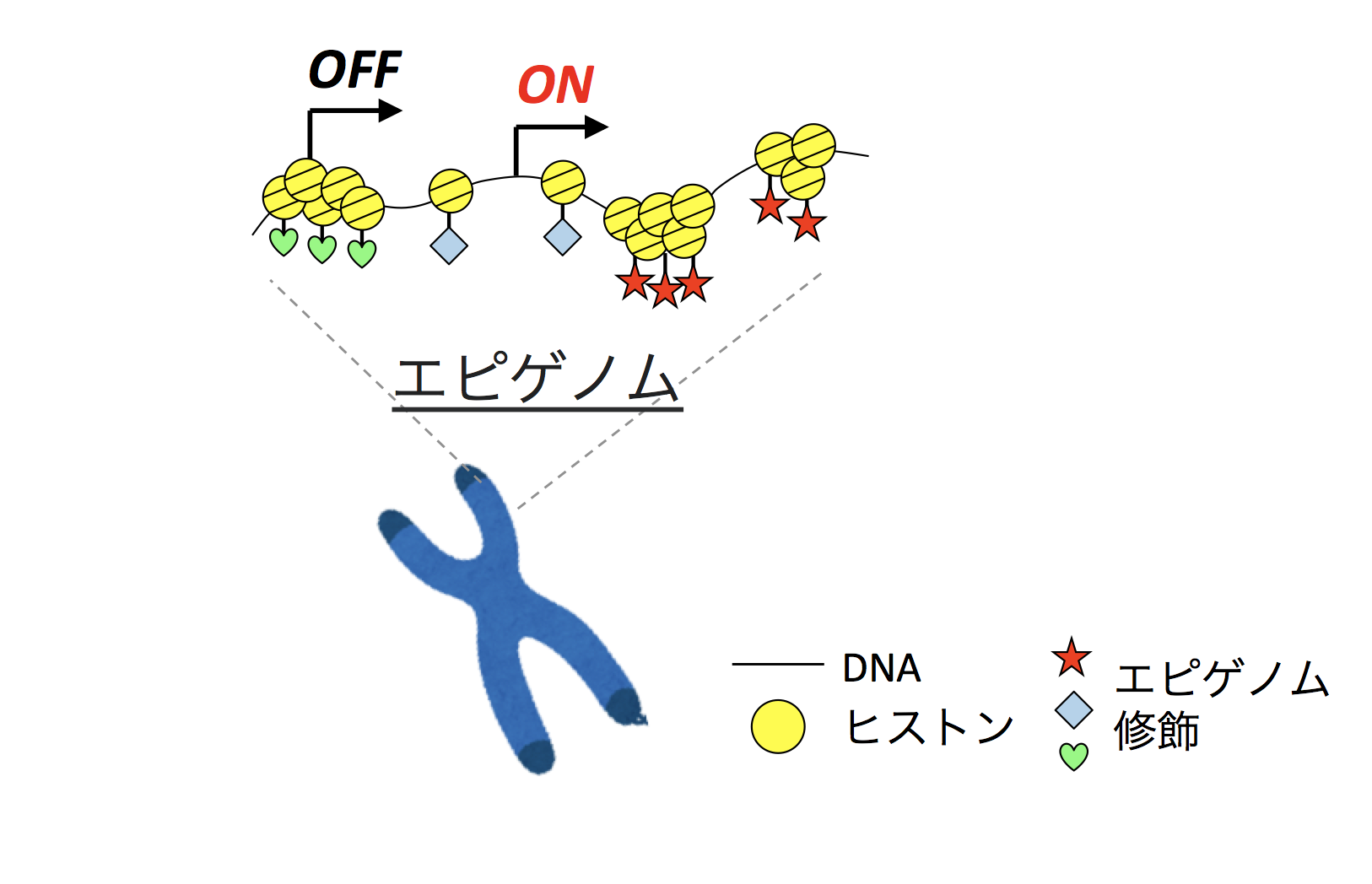 ヒストン修飾の分布や、ヌクレオソームの位置を含むクロマチン構造は、環境の変化などに応じて刻々と変化している
ヒストン修飾の分布や、ヌクレオソームの位置を含むクロマチン構造は、環境の変化などに応じて刻々と変化しているたとえば栄養が豊富な環境にいるときは、栄養過多にならないよう「栄養の吸収を抑制する遺伝子」に「転写を活性化する修飾」が入ります。細胞が受けた刺激の応答として、化学修飾が施されているのです。
現在のエピゲノム情報が「過去の刺激」に応答した結果なら、それは細胞の過去を表していることになります。さらに、クロマチン構造がオープンになっている部分の遺伝子は「現在転写可能」もしくは「今後転写可能」という状態であるため、細胞の未来が予測可能であり、制御できる可能性を秘めています。
そのため私は、エピゲノム情報から個体の老化やストレスなどの経験を読み取り、書き換えることによって、低下した機能の回復や、疾患の予防・治療などに貢献できると考えています。
私たちの認知機能や記憶力は成長とともに向上し、老化によって低下します。また、老化した脳は、アルツハイマー病や脳梗塞などの神経系疾患を発症しやすくなります。
短期間で入れ替わる皮膚細胞とは異なり、脳を構成するニューロンのほとんどは生まれてから死ぬまで入れ替わりません。このことから、ニューロンの機能の変化は、加齢によるエピゲノム情報の変化に起因すると考えられます。
しかし、これまで包括的にニューロンのエピゲノム情報を解析した報告はそれほど多くありません。ニューロンには長い突起があり、採取の際に突起部分がちぎれて死んでしまい、うまく回収できないからです。
そこでニューロンの核のみで発現する特異的なたんぱく質を染色し、高効率にソートする手法を用いています。生体マウスの1つの皮質から100個以上のニューロン核が安定的に回収可能となったため、本研究に着手できたのです。
 エピゲノム情報は細胞の「過去」「現在」「未来」を記憶・制御するというテーマのもと、研究に取り組んでいる
エピゲノム情報は細胞の「過去」「現在」「未来」を記憶・制御するというテーマのもと、研究に取り組んでいる