理化学研究所 生命機能科学研究センター 先端バイオイメージング研究チーム チームリーダー
再生医療への迅速な応用展開を図るためです。
現在の技術では、細胞の遺伝子発現パターンを調べるには、侵襲的な方法しかありません。それは細胞を壊してしまうため、再生医療への応用が不可能でした。
しかしこの方法なら、光を当てるという非侵襲的な手法で、遺伝子発現を予測することができます。iPS細胞のリプログラミングの成熟度をはじめとする品質評価や分化能評価が可能になり、その他の細胞のさまざまな機能評価にも活用できます。
その通りです。従来の研究では、得られたデータに対して人間が定義付けを行い、その上で議論をしていました。
この研究では、複雑なデータを複雑なまま扱うことで、人間の思考がもたらすバイアスを排除しています。機械学習によるクラスタリングにおいても、非線形の深層学習ではなく、線形の相互作用の組み合わせのみで判断するPLSを採用しています。
データの定義を人間ではなく機械学習が行い、私たちはそれを確認し、解釈して、次に行うべきことを決める。人工知能が膨大なデータを処理できるようになったことから、今後はこのようなデータ駆動型サイエンスが主流になると考えています。
「ラマン散乱スペクトルによってiPS細胞の種類の区別ができることの確認」「相関クラスタリングの試行」「遺伝子発現予測の試行」を実施するため、17種類のiPS細胞を対象に、1種類につき200個のラマン散乱スペクトルデータの収集と、RNAシーケンス解析を行いました。
残念ながら17種類のiPS細胞のラマン散乱スペクトルはほとんど同じで、区別することは困難でした。それでもRNAシーケンスデータの相関クラスタリングによって、いくつかの遺伝子発現がラマン散乱スペクトルの形状と相関があることが明らかになりました。また、この方法ではRNA発現パターンの推定には至らなかったものの、相関の強いラマン散乱スペクトルピークと遺伝子発現を同定し、相関の強い箇所を抽出したデータで機械学習を行えば、遺伝子発現パターン推定の精度向上が見込めます。
ただし、領域代表者の先生からは「結果がわかりにくいiPS細胞ではなく、別の細胞を使ったほうがいい」と助言をいただいたので、今後は別の細胞で実験系を再構築し、データ収集や機械学習手法の改良に取り組んでいきます。
予想していた結果は得られませんでしたが、実現可能性は証明できました。
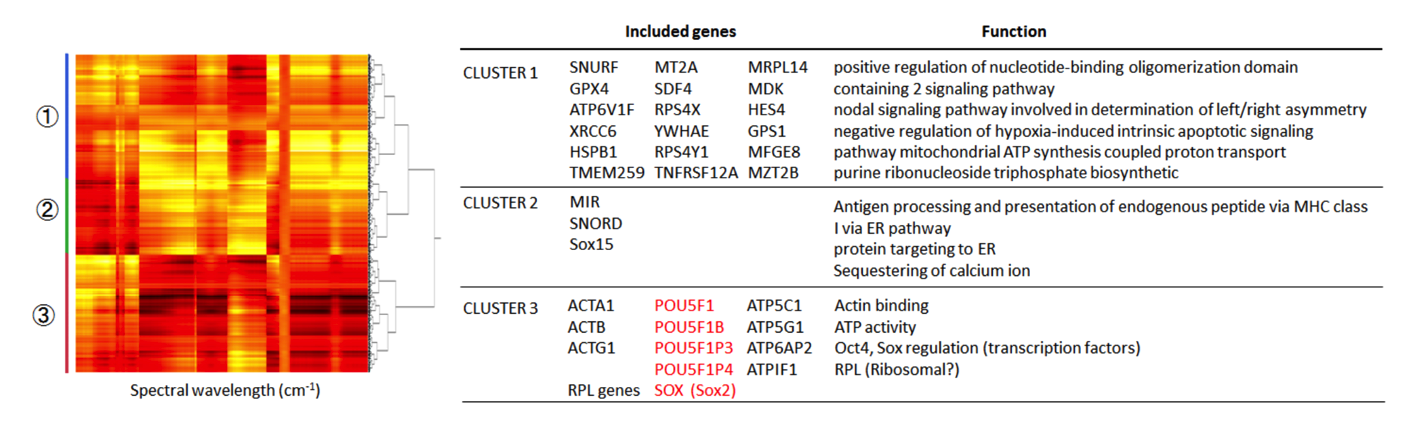 相関クラスタリング(左)とクラスターに寄与する遺伝子と関連機能(右)
相関クラスタリング(左)とクラスターに寄与する遺伝子と関連機能(右)これまで、この研究は「重要性は理解できるし、面白い研究だとは思うが、実現可能性が見えない」と言われ、なかなか研究費を獲得することができませんでした。
実現可能性が分からないのは、誰も挑戦していないからです。確かに私はAIも機械学習も素人ですが、可能性の有無を確かめるためには、実際に研究を行うしかない、そのために研究をさせてほしいと、ずっと願っていました。
今回、セコム科学技術振興財団から助成金をいただいたおかげで、ようやくスタートすることができました。また、面接の時には桜田先生から「アメリカではこうした研究が進んでいるが、日本では君たちだけだ。急ぎ、研究を進めてほしい」というお言葉をいただき、大きな勇気をいただきました。心から感謝しています。
 研究をするのは、論文を書くためや賞を獲るためではなく、自分の知りたいことを明らかにするため、と語る渡邉先生
研究をするのは、論文を書くためや賞を獲るためではなく、自分の知りたいことを明らかにするため、と語る渡邉先生