
理化学研究所 生命医科学研究センター 炎症制御研究チーム
チームリーダー

1989年奈良県立医科大学卒業。大阪大学医学部附属病院第3内科、大阪南医療センター内科にて研修医として勤務し、1995年に大阪大学医学部大学院医学研究科博士課程を修了。同年大阪大学細胞生体工学センター 免疫系形態形成研究分野の研究員となる。その後、兵庫医科大学生化学教室研究員、Harvard School of Public Health客員研究員を経て、2000年に同大学リサーチアソシエイトに。2004年には理化学研究所 免疫アレルギー科学総合研究センター生体防御研究チームの研究員となり、同研究センター炎症制御研究ユニットのユニットリーダー、統合生命医科学研究センター炎症制御研究チームのチームリーダーを経て、2018年に生命医科学研究センター炎症制御研究チームのチームリーダーに就任し、現在に至る。
私は、炎症反応を専門に研究しています。炎症反応とは、体内に細菌やウイルスなどの異物が入ったときに生じる、生体の防御反応のことです。感染部位の血流を増やして免疫細胞を動員することにより、体内に侵入した病原体を排除しますが、このときに発熱や痛みを伴います。
身体に悪影響を及ぼしている印象を受けますが、生体にとっては必須なものです。風邪を引けば炎症反応によって熱が出て、1週間ほどすれば治りますが、人によってはこの炎症反応が、時間が経っても治らずに継続することがあります。自己免疫疾患やアレルギーは、このような炎症反応が過剰になった状態と考えられます。
自己免疫疾患で苦しむ患者を診療しているうちに、根本的に治療法を見つけ出すことで患者を救いたいと考えたのが、研究者になったきっかけです。
 炎症反応は異物に対する防御反応であり、生体にとって必須なものである
炎症反応は異物に対する防御反応であり、生体にとって必須なものであるウイルスの根絶によって炎症反応が治まっていくのは、生体内の「炎症を負に制御するシステム」が働くからです。自己免疫疾患は、このシステムに異常をきたしている状態と仮定し、研究を始めました。まずはこの説明とともに、特定領域研究助成の申請に至った経緯についてお話しします。
炎症反応の発動には、「NF−κB」という核内の転写因子の活性化が重要であることが知られています。NF−κBは普段細胞質に存在していますが、活性化されると核内に移動し、炎症性サイトカインなどの炎症反応に必要な様々な遺伝子を活性化させ、炎症反応を誘導します。一方で、NF−κBが過剰発生すれば、炎症性疾患や自己免疫疾患を発症させる原因にもなるのです。
私は1998年に、2万個の遺伝子の中から網羅的解析を行い、ハーバード大学でPDLIM2(PDZ and LIM domain protein−2)という遺伝子が、NF−κBの分解を誘導することで炎症反応を抑制していることを発見しました。NF−κBにユビキチンというタンパク質を付加する(ユビキチン化)と、タンパク質分解酵素の標的になり、NF−κBが分解され、炎症反応が抑制されるという仕組みです。
そこでPDLIM2欠損マウスを作成したところ、肝臓が真っ白になる病変を起こしました。解析の結果、これはNASHであることがわかりました。
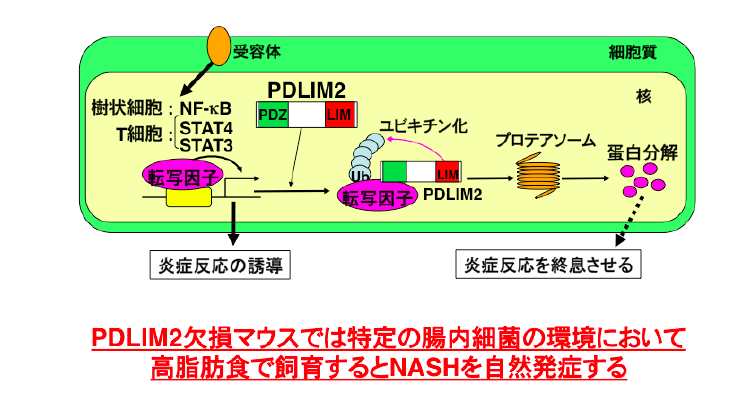 PDLIM2は核内転写調節因子NF−κBを分解して、炎症反応を終息させる
PDLIM2は核内転写調節因子NF−κBを分解して、炎症反応を終息させる肝臓に脂肪が多く溜まり、肝臓が白くなる状態を脂肪肝といいます。お酒を飲み過ぎた人に脂肪肝が起きることはよく知られていましたが、お酒を飲まない人にも同様の脂肪肝が起きることがわかり、「非アルコール性脂肪性肝疾患(NAFLD:NonAlcoholic Fatty Liver Disease)」と呼ばれています。
NAFLDのうち、80〜90%は長い経過を見ても脂肪肝のままであり、ほとんど進行することはありません。これを単純性脂肪肝といいます。しかし、残りの10〜20%の人は炎症反応や繊維化が徐々に悪化して肝硬変に進行したり、なかには肝がんを発症したりすることが最近わかってきました。この脂肪肝から徐々に進行する肝臓病のことを「非アルコール性脂肪肝炎(NASH:NonAlcoholic Steato-Hepatitis)」といいます。たとえNASHになっていても、自覚症状で単純性脂肪肝とNASHを区別することは困難です。また病気の原因も不明なため、確実な治療法がないのが現状です。
しかし、日本に戻り、理化学研究所でPDLIM2欠損マウスを作成したところ、肝臓はNASH病態を呈さない、通常色のままでした。