はい。人工的に肝臓にがんを転移させたマウスモデルに対して、合成RNAリガンドを投与したケースと、ドキソルビシンを投与したケースで、肝臓の組織を比較してみました。
すると、ドキソルビシンを投与した肝臓細胞は、がん細胞以外の広い領域で細胞死が見られましたが、合成リガンドを投与した場合は、がん細胞の領域のみ細胞死が起こっていました。
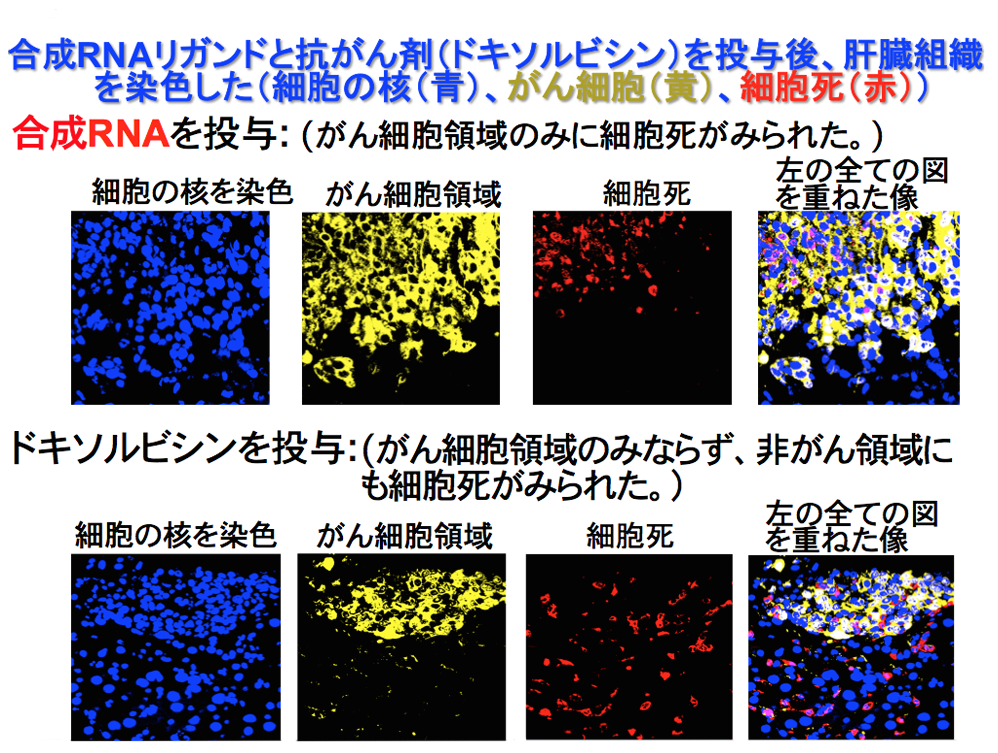
合成RNAリガンドの投与はがん細胞だけに細胞死を誘導し、正常細胞には大きな影響を与えないことが生体レベルでも確認できた
また、肝臓の腫瘍に2日おきに合成RNAを投与したマウスは、腫瘍が徐々に小さくなり生命を維持しましたが、投与しなかったマウスは腫瘍が大きくなり、30日後に死亡しました。これにより、この合成RNAの投与は生体においてもがん細胞に特異的に作用し、腫瘍を縮小させる効果があると期待できます。
さらに「がん幹細胞」に対しても、この合成RNAががん細胞と同様に細胞死誘導効果があることを確認しました。
そうです。がん幹細胞は抗がん剤が効きにくいという性質があるため、化学療法で腫瘍が縮小し、治癒したように見えても、それが体内に残っている限りは再発の危険があります。しかし合成RNAの投与が、がん幹細胞にも有効であるなら、このリスクも軽減できる可能性があります。
さらに、次のような実験を行いました。
がんを発症させたマウスに合成RNAを投与し、腫瘍がほぼ消失した状態にしてから、再度同じがん細胞を移植しました。通常であればがん細胞の増殖が始まり、がんが形成されて再発します。しかしこのマウスでは、新たながんの形成が見られませんでした。
この結果から、この合成RNAの投与によって適応免疫系が活性化し、このがん細胞に対する免疫がつくられたと推測できます。
実験から多くの有効なデータを得ることができましたが、なぜがん細胞のみに作用するのか、どのように細胞死を誘導しているのか、そのメカニズムに関して、分子レベルで突き詰める必要があります。
この合成RNAによって活性化した自然免疫核酸センサーが細胞内にシグナルを伝達するとアダプター分子や転写因子群が活性化されて、さまざまなサイトカインなどの遺伝子の発現が誘導されます。
今回見出したこの合成RNAによる細胞死の誘導が、この従来のシグナル伝達経路を介して生じているのか、それとも別のシグナル経路によって細胞死が起こるのか。それを確認することが、次の課題になりました。

新しいがん標的化モジュールの提言を目指し、自然免疫系の研究者としてこのメカニズムの解明に挑む
 合成RNAリガンドの投与はがん細胞だけに細胞死を誘導し、正常細胞には大きな影響を与えないことが生体レベルでも確認できた
合成RNAリガンドの投与はがん細胞だけに細胞死を誘導し、正常細胞には大きな影響を与えないことが生体レベルでも確認できた



 新しいがん標的化モジュールの提言を目指し、自然免疫系の研究者としてこのメカニズムの解明に挑む
新しいがん標的化モジュールの提言を目指し、自然免疫系の研究者としてこのメカニズムの解明に挑む