糖尿病の治療法の一つであり、血糖値をコントロールする治療法として最も有効なインスリン療法。従来の注射によるインスリン投与のほか、マイクロコンピュータ制御により持続的にインスリン投与を行う装置や、生体由来の素材を用いたエレクトロニクスフリーデバイスの開発など、世界中で研究が進められています。
第2回のインタビューでは、内分泌・糖尿病内科と生体材料工学の医工連携チームが開発したスマートインスリンデバイスの最新モデル、および実用化までの道程や課題について、ご説明いただきます。
前回のおさらいとして、従来のインスリン療法の課題と、先生が開発された「スマートインスリンデバイス」の概要について、もう一度簡単に教えていただけますか。
従来のインスリン療法は、患者が自分で注射を打たなくてはならないため日常生活における負担が大きく、食後の血糖値上昇に応じたインスリン投与が困難であり、低血糖のリスクを回避するために投与量が少なくなってしまうなど、多くの課題がありました。
そのため本研究では、周囲のグルコース濃度の変動によって形態がダイナミックに変化する「グルコース応答性ゲル」を活用することで、血糖値の変動を持続的にモニタリングし、適量のインスリンが自動的に投与される「スマートインスリンデバイス」の開発を進めています。
内分泌・糖尿病内科の私の研究チームと、生体材料工学の松元亮先生のチームで力を合わせて、はじめにカテーテルモデル、次に中空糸融合型のモデルと、課題点を克服しながら改良を重ねてきました。

松元先生の生体材料工学の専門知識なしに、新しいモデルは生まれない
まさに異分野のエキスパートによる、コラボレーションの成果ですね。
中空糸融合型モデルの完成により、インスリン供給の効率化が大幅に進みましたが、臨床応用に至るまでには、まだまだ課題がありました。
まず、皮下に埋め込む装置である以上、定期的に皮膚を切開して装置を交換する手術が必要になります。さらに、何らかの物理的衝撃によって体内でデバイスが破損した場合、大量のインスリンが放出されて低血糖状態に陥るリスクもあります。
これらの課題を解決するためには、皮下に埋め込むのではなく、外部からインスリンを投与するモデルに変更する必要がありました。そうして誕生したのが「マイクロニードル融合型デバイス」です。
マイクロニードルという名称は、初めて聞きました。
マイクロニードルは、長さが1㎜未満の微細な針です。先端部に薬剤を含有させ、シート上に剣山状に並べた状態で皮膚に貼り薬剤投与を行う、パッチ型の新しい経皮吸収技術です。針が痛点まで達しないため「痛みを感じない」というメリットがあり、予防接種をはじめ幅広い活用が期待され、注目されています。
マイクロニードル融合型デバイスは、マイクロニードルの先端部をグルコース応答性ゲルでコーティングし、これを皮膚に貼ることで、継続的なインスリン投与を行います。原理はこれまでと全く同じですが、侵襲性が大幅に低減し、交換が容易になりました。また、インスリンサーバーが体外にあることから、万が一破損しても外部に漏れるだけなので、低血糖のリスクも回避できます。

マイクロニードル融合型デバイスのイメージ図(左)、現在開発中のプロトタイプ(右)
バンドエイドのように「皮膚に貼るだけ」なら、インスリン療法に対するハードルが大きく下がりますね。ただ、マイクロニードルが皮膚のごく浅い部分にしか刺さらないのであれば、どのようにして血糖値を感知し、放出されたインスリンはどうやって血管まで到達するのでしょうか。
とてもいい質問です。細胞は血液の成分に触れていなければ生きていけないため、血管から染み出して組織を環流する「間質液」に浸された状態にあります。この間質液に到達することで血糖値を感知し、放出したインスリンは間質液を通して血管内に届けられていると考えています。
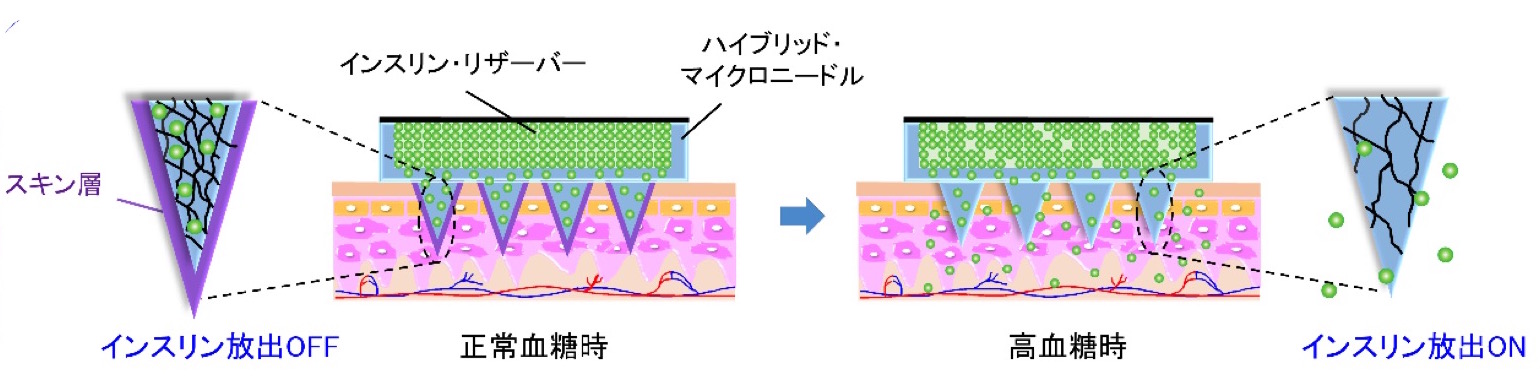
マイクロニードルが血管まで到達しなくても、インスリンは血液まで届けられる
ただし、マイクロニードルはまだ新しく、解明されていない部分が多い技術です。たとえば気温の変動による皮膚状態や血流の変化に対する影響などは、今後の研究によって明らかにしていく必要があります。
 松元先生の生体材料工学の専門知識なしに、新しいモデルは生まれない
松元先生の生体材料工学の専門知識なしに、新しいモデルは生まれない

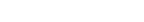
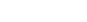

 マイクロニードル融合型デバイスのイメージ図(左)、現在開発中のプロトタイプ(右)
マイクロニードル融合型デバイスのイメージ図(左)、現在開発中のプロトタイプ(右) マイクロニードルが血管まで到達しなくても、インスリンは血液まで届けられる
マイクロニードルが血管まで到達しなくても、インスリンは血液まで届けられる