最初に製作したのは、マウス用のデバイスです。シリコン製カテーテルの内部にインスリン充填部を設置し、その周囲をグルコース応答性ゲルで覆って、カテーテル表面に小さな穴を空けました。血糖値が高いときはゲルが柔らかくなり、表面の穴からインスリンが外部に放出される。血糖値が正常値まで下がるとゲルの表面にスキン層が形成されて、インスリンの放出が止まる、という仕組みです。
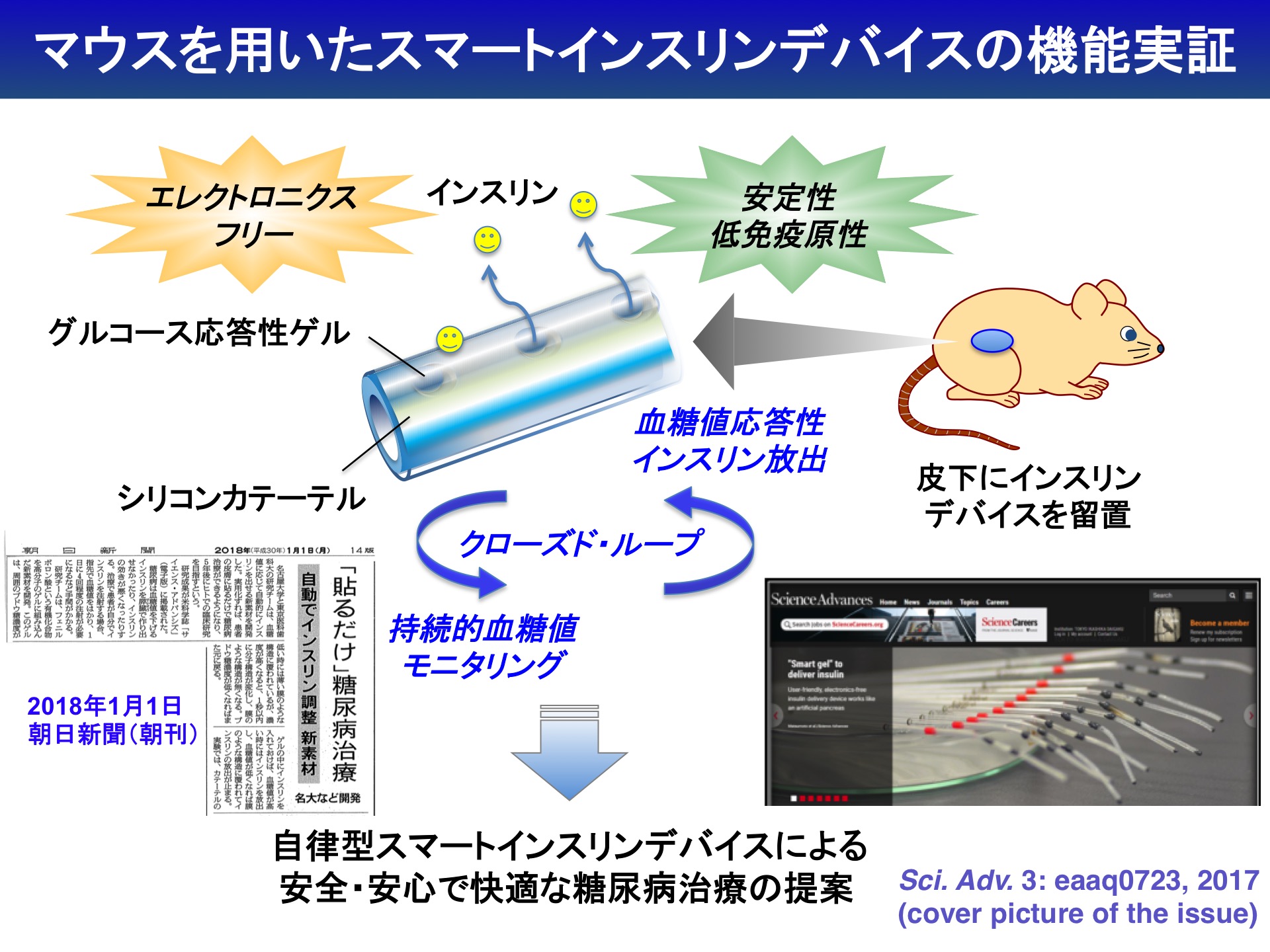
グルコース応答性ゲルの形態変化により適量のインスリンが放出され、連続的・長期的・自律的にインスリン供給を行う
これをマウスの皮下に埋め込み、食事の代わりにグルコースを注射して、実験しました。すると、通常のマウスはグルコース注射によって血糖値が大きく上昇しましたが、デバイスを埋め込んだマウスの血糖値上昇は抑えられました。
そのまま実験を続けた結果、少なくとも3週間はデバイスが血糖値上昇に反応して効果が持続すること、副作用がないことも確認できました。グルコース応答性ゲルが血糖値を持続的にモニタリングし、必要な量のインスリンが投与され続けたのです。
解決すべき課題はたくさんあります。まず、ヒトはマウスより体重が1000倍重いため、このモデルのスケールアップが必須でした。
そこで次に、マウスの10倍の体重を持つラットで実験を行いました。その結果わかったことは、マウスと同じ効果をラットで得るためには、6個のデバイスを埋め込む必要があるということです。
これでは、とても人間に適用できません。かなりショックでしたが、デバイスの根本的な作り直しに着手しました。小さな面積でインスリンを効率的に投与するために、松元先生とともに試行錯誤を重ね、中空糸(ちゅうくうし)を使った新しいモデルにたどり着いたのです。

中空糸モデルを考案するまで、まさに苦心惨憺の道のりだった
腎不全患者を治療する血液透析で用いられている半透膜の材料で、小さな分子は通過しますが、大きな分子は通さない性質を持っています。この中空糸とグルコース応答性ゲルを融合させ、インスリンリザーバーと結合させることで、カテーテルモデルの何百倍もの表面積でインスリンを放出できるようになりました。
この中空糸融合モデルをラットの皮下に埋め込み実験したところ、デバイス1個のみで効果が現れました。
また、新しい発見もありました。スマートインスリンデバイスは食後の一時的な血糖値上昇を抑えるだけではなく、持続的な効果をもたらすことにより、血糖値変動(血糖値スパイク)を減少させることが確認されました。従来のインスリン療法では対応できなかった領域の課題に対し、長期的・自律的なインスリン供給による解決の可能性が見出されたのです。
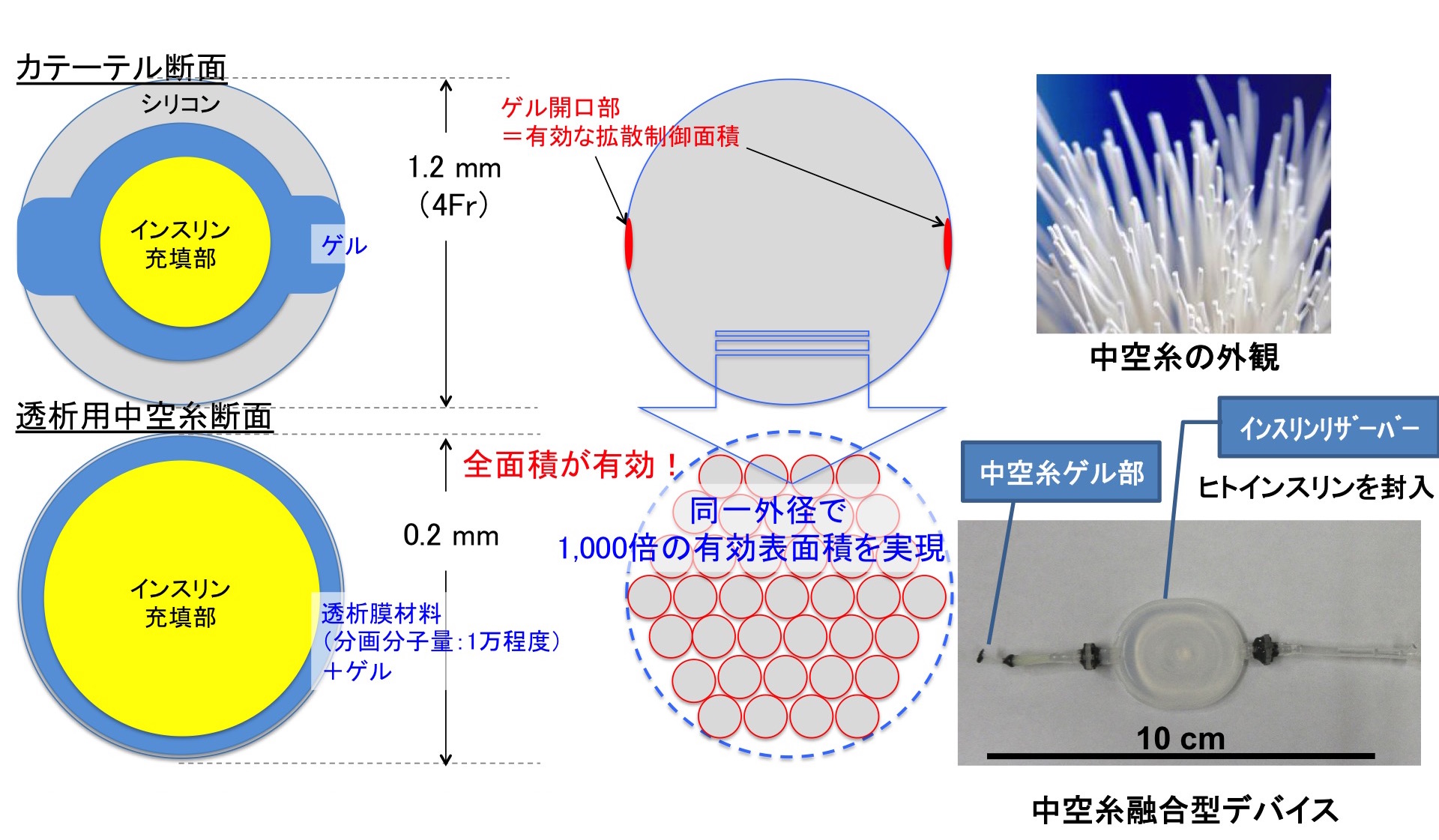
中空糸融合型インスリンデバイスの作製。複数の中空糸を束ねることで、インスリンの放出効率が大幅にアップした
 グルコース応答性ゲルの形態変化により適量のインスリンが放出され、連続的・長期的・自律的にインスリン供給を行う
グルコース応答性ゲルの形態変化により適量のインスリンが放出され、連続的・長期的・自律的にインスリン供給を行う



 中空糸モデルを考案するまで、まさに苦心惨憺の道のりだった
中空糸モデルを考案するまで、まさに苦心惨憺の道のりだった 中空糸融合型インスリンデバイスの作製。複数の中空糸を束ねることで、インスリンの放出効率が大幅にアップした
中空糸融合型インスリンデバイスの作製。複数の中空糸を束ねることで、インスリンの放出効率が大幅にアップした