脂肪細胞から分泌されたレプチンは、神経回路を介して脳の視床下部に作用することで、食べる量が調節されます。加えて、脂肪細胞は交感神経の伸長や密度上昇を促す栄養因子も出しています。この交感神経から分泌されるホルモンには、脂肪細胞の燃焼を助ける物質が含まれており「脂肪燃焼しやすい体質」づくりに関わっていることが報告されています。
つまり、摂食とエネルギー消費の制御は、中枢神経回路と脂肪細胞のネットワークを介していると考えることができるのです。
エピゲノム変化は細胞の核の中の出来事ですが、細胞の外には他の細胞があり、神経で繋がっています。すべての細胞は、外の環境に反応し、その反応も細胞同士で影響し合って核の中にあるエピゲノムに届いています。そうした細胞間相互作用、臓器間相互作用の中で、エピゲノムが摂食調節や脂肪燃焼にどのように関与しているのかを解明する必要があるのです。
 従来の研究では、エピゲノム、転写経路、RNA修飾が、それぞれ別のレイヤーとして扱われてきた。本研究ではそれらの相互作用を対象とし、急性期と慢性期の異なる時間軸における遺伝子発現と代謝制御の機構を明らかにする
従来の研究では、エピゲノム、転写経路、RNA修飾が、それぞれ別のレイヤーとして扱われてきた。本研究ではそれらの相互作用を対象とし、急性期と慢性期の異なる時間軸における遺伝子発現と代謝制御の機構を明らかにする

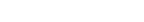

 ヒストン脱メチル化能不全マウスは寒冷刺激を与えられても、エピゲノムの書き換えが起きず、褐色化しないことがわかった
ヒストン脱メチル化能不全マウスは寒冷刺激を与えられても、エピゲノムの書き換えが起きず、褐色化しないことがわかった