胎児期に母親から供給される栄養が不足していた場合、飢餓状態でも生きられるよう、エネルギーの消費を抑えて栄養を蓄える体質が作られます。そのため、生まれる前の栄養状態が悪かったにもかかわらず、出生後に十分な栄養を与えられて育つと、肥満になりやすくなり、糖尿病や高血圧症を発症する可能性が高くなってしまうと考えられています。
ただし、これを科学的に証明することは、極めて困難です。

人間はいったん生まれたら同じ身体で生きていくにもかかわらず、「産婦人科」「小児科」「内科」「老年内科」のようにライフステージごとに別々の診療科と専門医が用意されています。しかし、生まれる前後の経験も含めた時間軸に沿った医療の実現には「過去に経験したことが現在の健康状態にどう影響しているか」という因果関係の証明が必要になります。
インタビュー第2回では、出生前後の環境因子を遺伝子上に記憶し、成人期の疾患の発症に影響を与える「エピゲノム記憶遺伝子」について、詳しく伺いました。
胎児期に母親から供給される栄養が不足していた場合、飢餓状態でも生きられるよう、エネルギーの消費を抑えて栄養を蓄える体質が作られます。そのため、生まれる前の栄養状態が悪かったにもかかわらず、出生後に十分な栄養を与えられて育つと、肥満になりやすくなり、糖尿病や高血圧症を発症する可能性が高くなってしまうと考えられています。
ただし、これを科学的に証明することは、極めて困難です。
そこで本研究では、生後4週間ほどで成獣になるマウスで実験を行いました。私たちが注目したのは、肝臓における代謝改善作用を持つホルモンFGF21への影響です。
前回お話ししたように、生まれる前は、FGF21遺伝子の働きはブロックされた状態(DNAメチル化)にあります。出生後、ミルクに含まれている脂肪酸が核内受容体PPARαを活性化させることでブロックが外れ(DNA脱メチル化)、肝臓は代謝機能を獲得します。
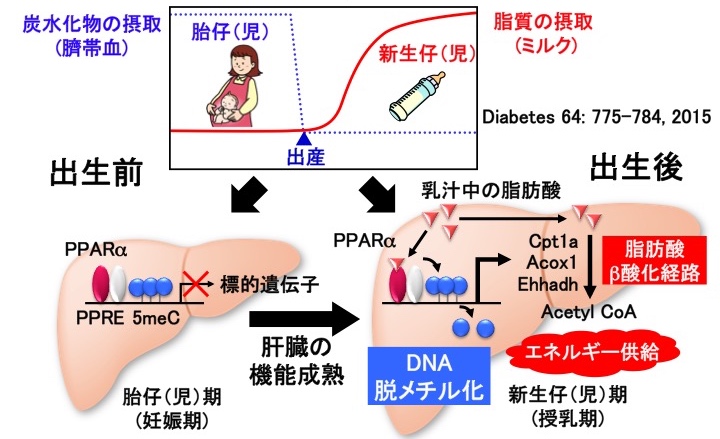 出生後、ミルクの摂取によって体内に入ってきた脂肪酸が核内受容体PPRAαを活性化させ、
出生後、ミルクの摂取によって体内に入ってきた脂肪酸が核内受容体PPRAαを活性化させ、はい。実験では「PPARα欠損マウス」「通常の産仔マウス」「Wy14648(PPARαを活性化させる薬剤)を投与された母獣マウスの母乳を摂取した産仔マウス」を用意し、それぞれのFGF21遺伝子のDNAメチル化率の経時変化を調べました。その結果が、下の図です。
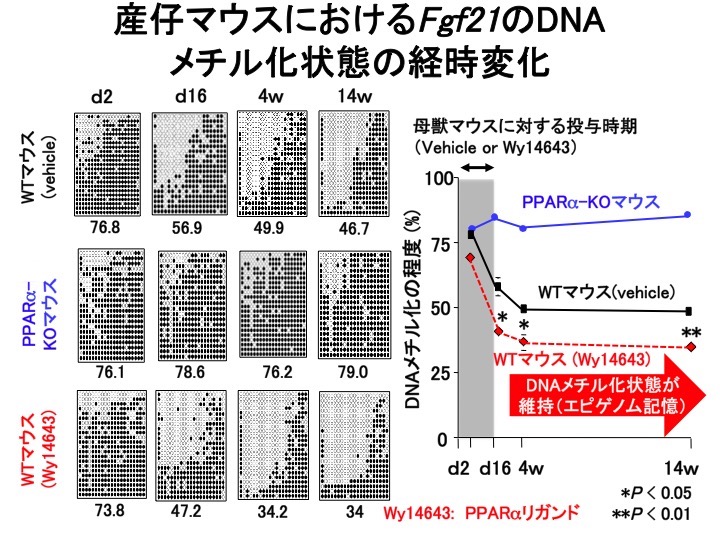 産仔マウスにおけるFGF21のDNAメチル化状態の経時変化。
産仔マウスにおけるFGF21のDNAメチル化状態の経時変化。
これは母獣マウスの母乳を介して、産仔マウスのPPARαが通常よりも活性化されたためと考えられます。
さらに注目すべきは、生後4週間を経過するとDNAメチル化率の低下が止まり、その後はほとんど変化しなくなる、ということです。
実験により、乳仔期に一度確立されたFGF21遺伝子のDNAメチル化状態は、成獣期にWy14648を投与しても変化しないことを確認しています。
つまり、マウスのFGF21遺伝子のDNAメチル化状態は「生後4週間の栄養環境」の影響を受けて確立されるものであり、かつ、その状態は成獣になっても変化することなく維持されるということです。
これによりFGF21遺伝子は、乳仔期に確立されるDNAメチル化状態が成獣期のエネルギー代謝制御に影響を与える「エピゲノム記憶遺伝子」のひとつであると考えられます。