組織や臓器はさまざまなストレスを受けることで、細胞が傷ついたり、遺伝子変異を起こしたりして、正常ではない「異常細胞」が生じます。この異常細胞を自ら排除する機構があるため、組織や臓器は恒常性を維持できていると考えられます。
代謝と解毒の中心臓器である肝臓の研究を長年続けてきた私たちは、哺乳動物培養細胞やマウスの肝臓を用いた実験・解析から、「Hippo-YAPシグナル伝達経路」が異常細胞の排除を誘導していること、異常細胞排除にはYAPの活性化と排除因子が必須であることを見出しました。
本研究では異常細胞排除に必要な因子を同定すること、そして異常細胞排除を誘導する因子の組み合わせを発見することで、人為的に異常細胞排除を誘導する、新たな治療法の開発を目指しています。
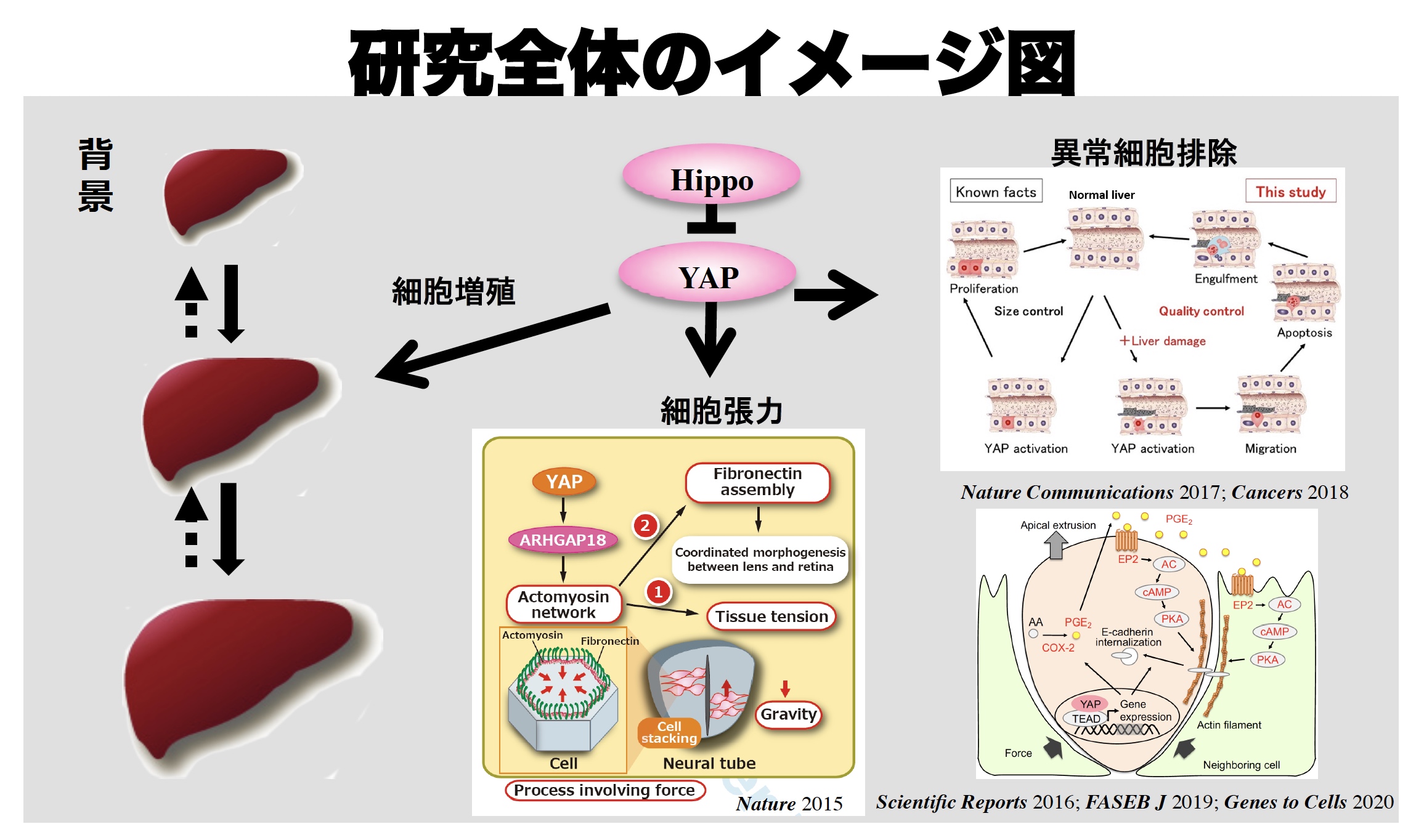
白血病などに適応される再生医療は「細胞補充」を基本とする。この研究では「細胞排除(除去)」という逆方向からのアプローチを目指す
はい、その通りです。マウスの肝臓は体重の約5%ですが、活性型YAPを導入して標的遺伝子を過剰に発現させると、肝細胞が増殖して、肝臓は体重の約25%、つまり5倍の大きさに変化し、2カ月後には肝臓はがん化します。
一方で、活性化の程度を弱めたYAPを導入すると、細胞排除は誘導されましたが、肝臓のサイズ変化は生じず、肝がんも発症しませんでした。つまりYAPの活性化を適切にコントロールすることで、細胞排除機構だけを誘導することが可能であることが示唆されました。
また、肝臓サイズが正常よりも小さければ細胞増殖によって元のサイズへと再生し、過剰に大きくなる場合は細胞死を介した細胞排除によって適正サイズを維持する。実によくできた仕組みです。臓器が正常に機能するためには、細胞レベルの品質と適正サイズの維持が重要であることがわかります。
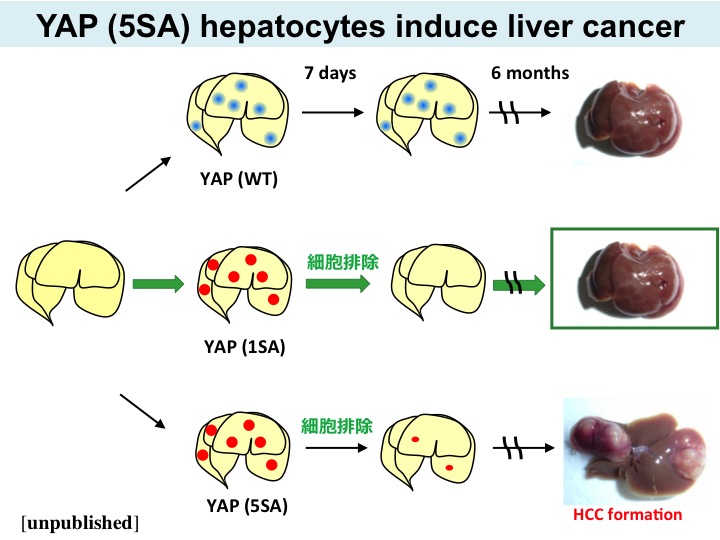
マウスの肝臓に活性型YAPを導入した実験。YAPの強い活性化状態が持続すると、異常細胞排除が間に合わずに、がん化すると考えられる
はい、その通りです。YAP誘導性の異常細胞排除は、細胞に傷害が生じたというシグナルを受けてスタートします。その細胞が「正常細胞ではない」ことが前提であるため、正常な肝細胞のYAPを持続的に活性化して過剰に遺伝子発現を誘導すると、恒常性を壊してしまうのです。
肝細胞が傷ついたとき、その刺激がどのようにして排除シグナルに変換され、どのようにYAP活性化と協調して排除機構が働くのか。これらをすべて明らかにしなければ、新たな治療法の開発には至れません。

「Hippo-YAPシグナル伝達経路」は肝臓のサイズ制御のみならず、品質制御など恒常性維持に関与することを見出した
 白血病などに適応される再生医療は「細胞補充」を基本とする。この研究では「細胞排除(除去)」という逆方向からのアプローチを目指す
白血病などに適応される再生医療は「細胞補充」を基本とする。この研究では「細胞排除(除去)」という逆方向からのアプローチを目指す


 マウスの肝臓に活性型YAPを導入した実験。YAPの強い活性化状態が持続すると、異常細胞排除が間に合わずに、がん化すると考えられる
マウスの肝臓に活性型YAPを導入した実験。YAPの強い活性化状態が持続すると、異常細胞排除が間に合わずに、がん化すると考えられる 「Hippo-YAPシグナル伝達経路」は肝臓のサイズ制御のみならず、品質制御など恒常性維持に関与することを見出した
「Hippo-YAPシグナル伝達経路」は肝臓のサイズ制御のみならず、品質制御など恒常性維持に関与することを見出した