そうです。白色脂肪細胞はエネルギーを貯蔵する細胞のため、エネルギーを産生するミトコンドリアの生合成量が抑制されています。これは、ゲノム上の「ミトコンドリアの生合成を活性化する遺伝子」に遺伝子の発現を抑制するメチル化という化学修飾が入り、遺伝子の発現が抑制されている、いわばストッパーがかかった状態です。
しかし寒冷刺激が慢性化し、褐色脂肪細胞が作る熱だけでは足りなくなり、白色脂肪細胞も熱を産生する必要が生じると、このストッパーが外れます。化学修飾が外れてエピゲノムが書き換わり、ミトコンドリアの生合成量が増加して高レベルでエネルギーを消費するベージュ脂肪細胞の性質に変化する、ということです。

一般的に、年齢を重ねるごとに太りやすい体質になる。ここにも、ミトコンドリアの生合成量の変化が関わっていると考えられている
寒冷刺激に対する急性期の反応では、褐色脂肪細胞が熱エネルギーをより多く産生するようになりますが、もとより褐色脂肪細胞は熱産生の機能があり、それが活性化された状態であるため、エピゲノムの書き換えは起きていません。
一方、慢性期では本来脂肪をため込む白色脂肪組織の脂肪細胞あるいは前駆脂肪細胞でエピゲノムの書き換えが起こり、細胞の「質の変化」をもたらします。脂肪貯蓄から脂肪燃焼細胞へ、運命決定が変わるのです。
急性期から慢性期への寒冷暴露に対する応答は、あたかも車の「ギアチェンジ」のようなイメージです。皮下脂肪組織ではスピード(熱)を出す必要がないためローギアでしか走れなかった車(褐色脂肪細胞のみが熱産生)が、高速道路に出たことでトップスピードが出るギアにチェンジ可能になった(皮下の白色脂肪組織も熱産生が可能な状態に変化)、ということです。
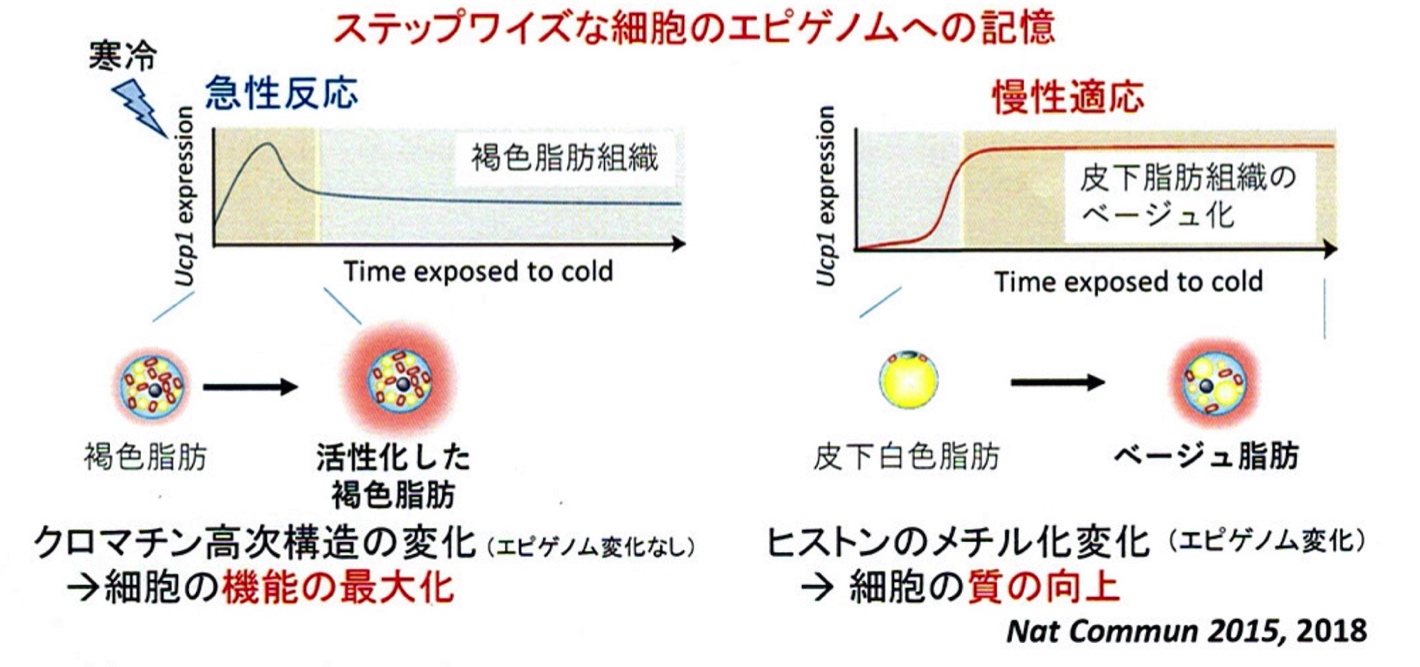
エピゲノムを介した環境変化への適応機構。脂肪細胞のエピゲノムは寒冷刺激に対し、急性期と慢性期で異なる反応を示す
そうです。肥満になりやすい体質から、なりにくい体質へと変えることができるはずです。そのためには、エピゲノムの観点から「哺乳動物の“肥満になりやすい体質”はどのように決定づけられるのか」を解明する必要があります。
そこで、まずは寒冷刺激に対する脂肪細胞の急性反応・慢性適応に関与しているエピゲノム酵素(ヒストン脱メチル化酵素)を持たないマウスを用いて、さまざまな実験を行いました。
その結果、このマウスは過食を伴う肥満になりました。加えて、レプチンに対する感受性が低いこともわかってまいりました。レプチンとは脂肪細胞から分泌される、摂食をコントロールするホルモンです。
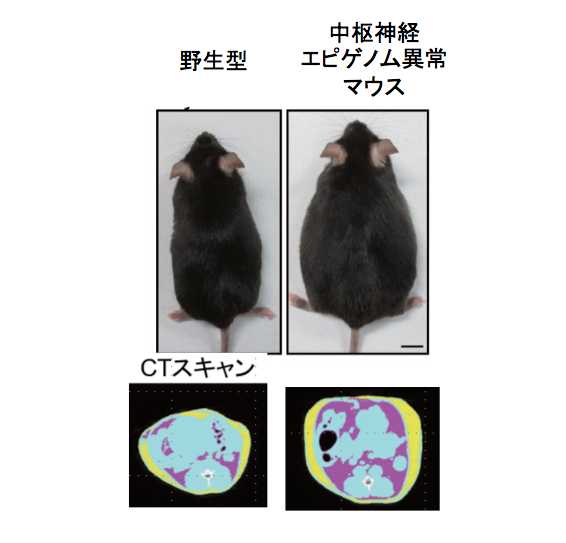
ヒストン脱メチル化異常マウスは、肥満と過食を呈した。エピゲノム異常が過食・肥満を引き起こす原因を解明することで、エピゲノム酵素が感知する環境からのシグナルを標的とした生活習慣病の予防法の開発に寄与する
 一般的に、年齢を重ねるごとに太りやすい体質になる。ここにも、ミトコンドリアの生合成量の変化が関わっていると考えられている
一般的に、年齢を重ねるごとに太りやすい体質になる。ここにも、ミトコンドリアの生合成量の変化が関わっていると考えられている

 エピゲノムを介した環境変化への適応機構。脂肪細胞のエピゲノムは寒冷刺激に対し、急性期と慢性期で異なる反応を示す
エピゲノムを介した環境変化への適応機構。脂肪細胞のエピゲノムは寒冷刺激に対し、急性期と慢性期で異なる反応を示す ヒストン脱メチル化異常マウスは、肥満と過食を呈した。エピゲノム異常が過食・肥満を引き起こす原因を解明することで、エピゲノム酵素が感知する環境からのシグナルを標的とした生活習慣病の予防法の開発に寄与する
ヒストン脱メチル化異常マウスは、肥満と過食を呈した。エピゲノム異常が過食・肥満を引き起こす原因を解明することで、エピゲノム酵素が感知する環境からのシグナルを標的とした生活習慣病の予防法の開発に寄与する