その通りです。これまで明らかになっていることはほんの一部に過ぎず、腸内細菌の機能の全容はまだ分かっていません。
腸内細菌研究に限ったことではありませんが、研究アプローチとして、特定の細胞や特定の分子に着目して、そこからある現象を捉え、生体全体への影響を見ていくという進め方があります。しかし私は、疾患病態や生理機能など、生体で大きな影響がある現象をまず見つけて、それに対するメカニズムに迫っていく方が好きなのです。この手法では、核心に迫るメカニズムをなかなか明らかにできなかったり、既知のメカニズムに行きついてしまったりする可能性もありますが、この現象の中に、創薬や実用化に繋がる発見があると信じて研究をしています。

生体で起きている現象から、メカニズムに迫る
人には100兆個ほどの腸内細菌が生息していると言われているのですが、大腸に最も多く存在しています。大腸にいる腸内細菌は、私たちが食べたもののうち、小腸から消化・吸収されなかったものを餌にしていますが、これらを消費する際に多様な代謝物を産生します。この代謝物が我々の健康や病気と深く関わっているのです。
まず小腸の仕組みからお話ししましょう。たとえば、お米に含まれるデンプンなどの多糖類(単糖が10個以上連なったもの)を食べた後は、小腸で発現するグルコシダーゼやアミラーゼという酵素によって、単糖(ブドウ糖など)と呼ばれる1つの糖になって小腸から吸収されていきます。この酵素は、多糖類の連結を切るハサミの役割を果たしています。すなわち、連なっている糖を切って、単糖にする働きをしているのです。
しかし、多くの単糖(ブドウ糖)が短時間で吸収されると、血糖値が上がってしまいます。それは糖尿病患者にとって良くない状態のため、この酵素の働きを阻害する薬が、糖尿病の治療薬として使われているのです。ちなみにこの阻害薬が、今回の研究で着目したα-グルコシダーゼ阻害剤(α-GI)という薬です。
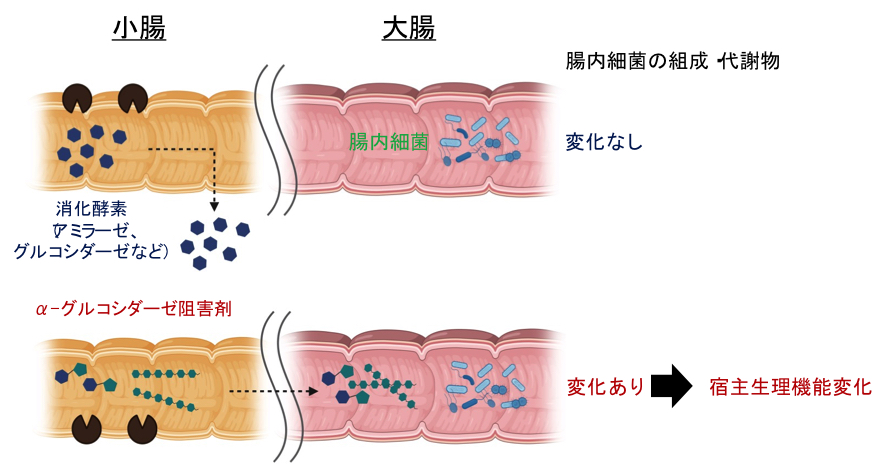
小腸(Small intestine)・大腸(Large intestine)の仕組み
小腸で消化吸収されなかったものは大腸に届いて、腸内細菌の餌になります。
先ほど食物繊維による研究結果についてお話ししましたが、食物繊維は難消化性の多糖類で、小腸では吸収されずに直接大腸に運ばれて、腸内細菌の餌になります。このような難消化性、あるいは難吸収性の糖類は腸内細菌によって消費されることから、「腸内細菌利用糖」と呼ばれています。
α-GIを投与した場合にも食物由来の多糖類が消化・吸収されずにこれらが腸内細菌利用糖として機能すると考えられます。そのため、α-GIを投与すると、腸内環境が変化し、アナフィラキシーの症状にも変化があるのでは、と考えました。
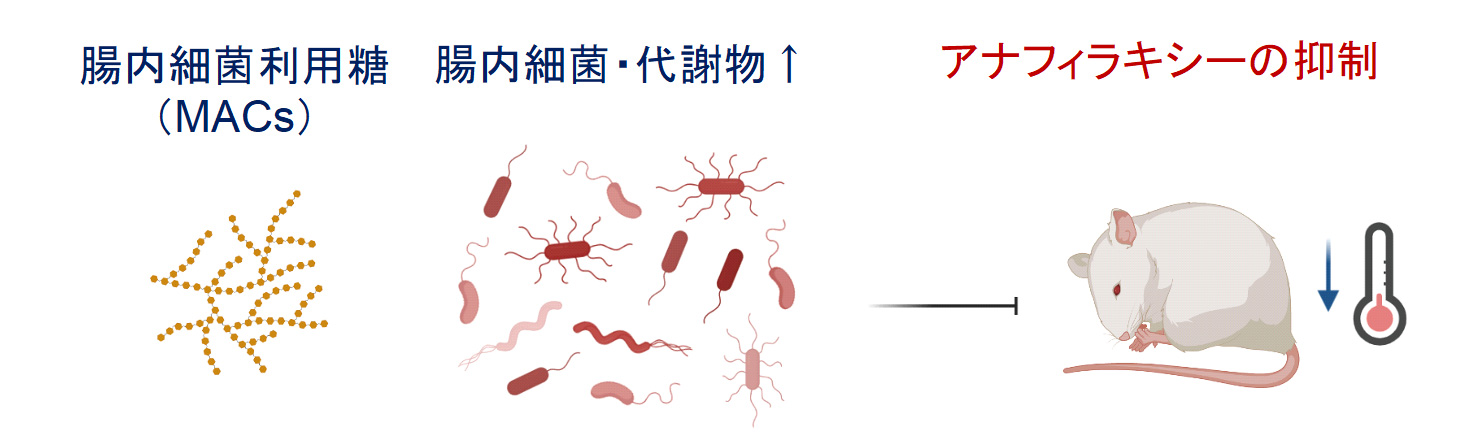
腸内細菌利用糖が腸内環境を変化させ、アナフィラキシーの抑制に繋がる
 生体で起きている現象から、メカニズムに迫る
生体で起きている現象から、メカニズムに迫る

 小腸(Small intestine)・大腸(Large intestine)の仕組み
小腸(Small intestine)・大腸(Large intestine)の仕組み 腸内細菌利用糖が腸内環境を変化させ、アナフィラキシーの抑制に繋がる
腸内細菌利用糖が腸内環境を変化させ、アナフィラキシーの抑制に繋がる