これまでの研究から、身体活動を14日間制限した成体のマウス(不動化マウス)は骨量が大きく低下すること、活動制限を解除した3日後に骨量が急激に回復し始めることがわかっています。通常の成体マウスでは観察されない速度で骨量が増加していく現象が起こるのです。
この現象を「超回復」と名付け、超回復が起こる期間を「回復期」と呼んでいます。
超回復の分子メカニズムを明らかにすることは、人為的な骨量増加方法の開発に繋がると考え、本研究では回復期に入ったマウス(不動化回復マウス)の骨組織で発現が有意に変動している遺伝子群の抽出を行っています。
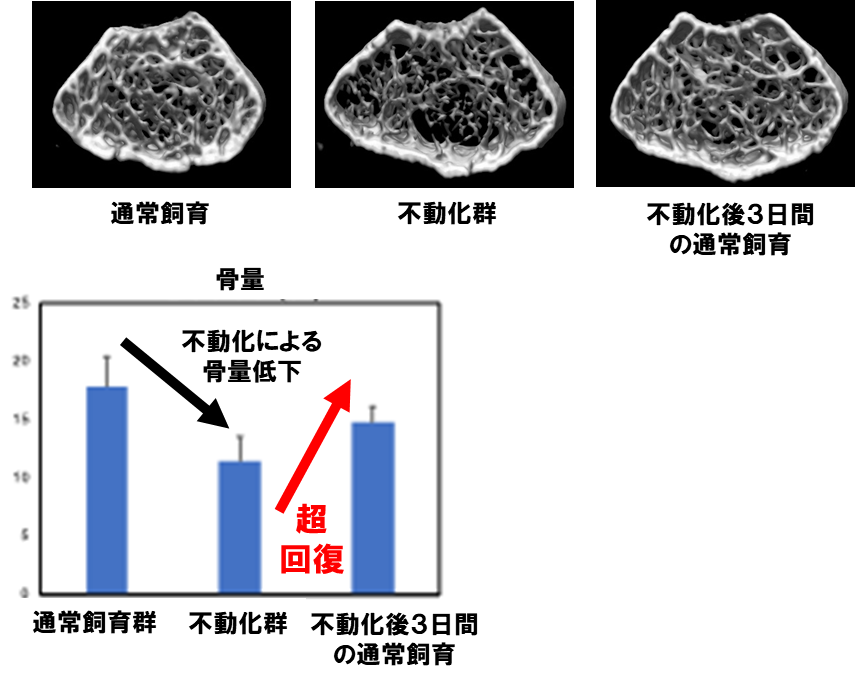
不動化による骨量低下と、短期間での超回復
はい。超回復においては骨吸収が著しく抑制されていることが判明したため、私はRANKLという破骨細胞分化因子の発現が低下していると考えました。そこで、RANKLを発現した細胞を対象に1細胞解析を行ったところ、回復期では骨組織の中でも特定の細胞群のみでRANKLの発現に変化が起きていることを発見しました。現在はこの細胞群に注目して、RANKL発現の分子メカニズムの解明を行っています。
ただし、創薬に貢献できる成果を出すためには、まだまだ時間がかかります。「運動」は、効果を実証できれば比較的容易に患者さんに実行してもらえるというメリットがあり、社会実装しやすいため、まずは予想システムと運動プログラムの開発に力を入れています。
マウスの実験データやヒトの臨床データを解析して仮説を立てた後は、再度マウスで実験を行い、再びデータを解析して検証する、いわば「裏を取る」作業が必要になります。
1回の検証で済めば良いのですが、結果に齟齬があったときはデータ解析のモデリング過程を見直して再び試みるなど、実験とデータ解析の往復を繰り返すことになります。
データ駆動型アプローチであればこのような作業は不要ですが、生物の疾患の進行や治療効果を定量的に予測するシミュレーションの構築には向いていません。時間がかかっても、モデル駆動型アプローチには検証作業が必須なのです。
しかし、良いこともあります。マウスの実験データとヒトの臨床データを行き来することで、両者に共通する傾向が見えてきました。実験を始めた当初は、マウスのデータをどのようにヒトに活かすべきか悩みましたが、今は大きな手応えを感じています。

すでに知られている現象の中にも、実験をして詳しく調べると「大枠は合っているがこの部分は違う」という結果が出ることもあるため、自分の手で確認する必要がある
 不動化による骨量低下と、短期間での超回復
不動化による骨量低下と、短期間での超回復

 すでに知られている現象の中にも、実験をして詳しく調べると「大枠は合っているがこの部分は違う」という結果が出ることもあるため、自分の手で確認する必要がある
すでに知られている現象の中にも、実験をして詳しく調べると「大枠は合っているがこの部分は違う」という結果が出ることもあるため、自分の手で確認する必要がある