- 所属
- 埼玉大学 大学院 理工学研究科 生命科学部門 分子生物学領域
- 職名
- 助教
- キーワード
- ノンコーディングRNA マイクロRNA RNAサイレンシング 免疫 核酸医薬
- 助成期間
- 平成31年度─令和3年度
- 2014年3月
東京大学 大学院 理学系研究科 生物化学専攻 博士後期課程修了・博士(理学)
- 2011年4月
日本学術振興会 特別研究員(DC1)
- 2014年4月
東京大学 大学院 理学系研究科 生物科学専攻 特任研究員
- 2014年8月
東京大学 大学院 理学系研究科 生物科学専攻 助教
- 2019年10月
埼玉大学 大学院 理工学研究科 生命科学部門 分子生物学領域 助教
高次生命機能への関連が注目されるノンコーディングRNA
新型コロナウイルスのワクチンに関する報道によって「メッセンジャーRNA」については、広く知られるようになりました。端的に言えば、DNAの情報の一部を転写してタンパク質を作るRNAが、メッセンジャーRNAです。
一方、タンパク質の情報を持たないRNAも存在します。これは「ノンコーディングRNA」と呼ばれています。
実はヒトゲノムの98%は、ノンコーディング領域が占めています。バクテリアなどのシンプルな生物ほどノンコーディング領域が少ないことから、近年、高次生命機能に関わる可能性や、重要な機能を持つRNAとして、注目を集めるようになってきました。私はノンコーディングRNAの中でも、塩基配列が短い「マイクロRNA」を研究対象としています。
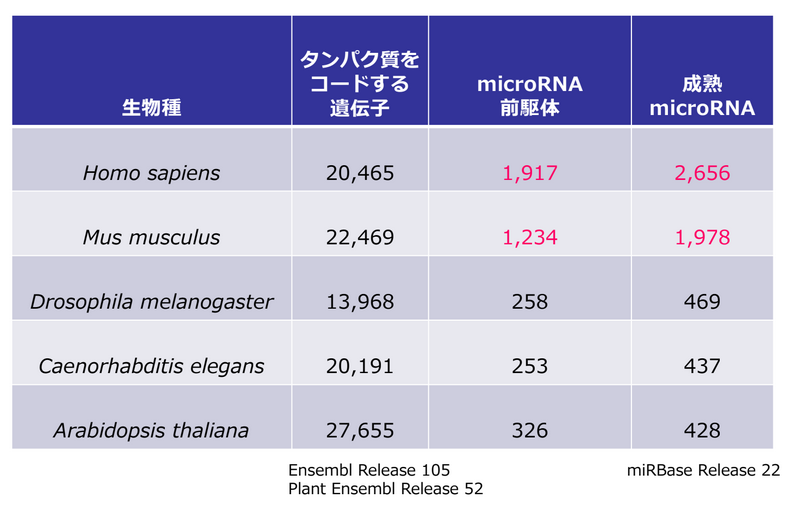 生物の遺伝子数には、大きな差はない。しかしマイクロRNAの種類は、無脊椎動物よりも哺乳類のほうがはるかに多く、さらに同じ哺乳類であってもマウスよりヒトのほうが多い
生物の遺伝子数には、大きな差はない。しかしマイクロRNAの種類は、無脊椎動物よりも哺乳類のほうがはるかに多く、さらに同じ哺乳類であってもマウスよりヒトのほうが多い遺伝子はRNAに転写された後、いくつかの行程を経て機能しますが、このマイクロRNAにはメッセンジャーRNAの遺伝子発現を転写後に抑制する「RNAサイレンシング」という働きがあります。
ヒトのマイクロRNAは現在知られているものだけでも2656種類あり、すべての組織で機能しますが、どのマイクロRNAが発現しているのかはそれぞれ異なります。つまり、同じ細胞であってもマイクロRNAの発現パターンが異なれば、その細胞機能も変化するということです。
 RNAサイレンシングの発見がノーベル生理学・医学賞を獲ったのは2006年。当時はまだ未知の部分が多く、学部生のころに強く興味をひかれた
RNAサイレンシングの発見がノーベル生理学・医学賞を獲ったのは2006年。当時はまだ未知の部分が多く、学部生のころに強く興味をひかれたヒトでもRNAによるRNAを標的とした免疫が作用するのか
ヒトをはじめとする哺乳類は、ウイルスが感染するとI型インターフェロン(IFN)などの抗ウイルス性サイトカインを分泌したり、免疫細胞がウイルスやウイルス感染細胞を排除することで、生体を守っています。これが感染後すぐに働く自然免疫の仕組みです。
植物や無脊椎動物はヒトのような免疫機構が発達していないため、侵入してきたウイルスRNAの情報から相補的な塩基配列を持つsiRNAを生成します。このsiRNAがウイルスRNAに結合すると、ウイルスの遺伝情報の発現が抑制され、ウイルス複製が起こらなくなります(これを抗ウイルスRNA干渉といいます)。
ヒトの細胞でも抗ウイルスRNA干渉の機構の一部は働いていますが、siRNAが生成されるのを阻害するメカニズムがいくつかあり、自然免疫や獲得免疫に対してどのような位置付けで、どのように働いているのかはわかっていません。ただ、siRNAによる抗ウイルスRNA干渉の仕組みは、マイクロRNAが遺伝子発現を転写後抑制する仕組みと、とてもよく似ています。
そのため私は、ヒトの細胞がウイルスに感染した際、マイクロRNAが、ヒトやウイルスのRNAをサイレンシングする “RNAによるRNAを標的とした免疫”の仕組みを明らかにすることで、ヒトの多様な免疫応答を決定づける分子基盤の解明に近づくことができると考えました。
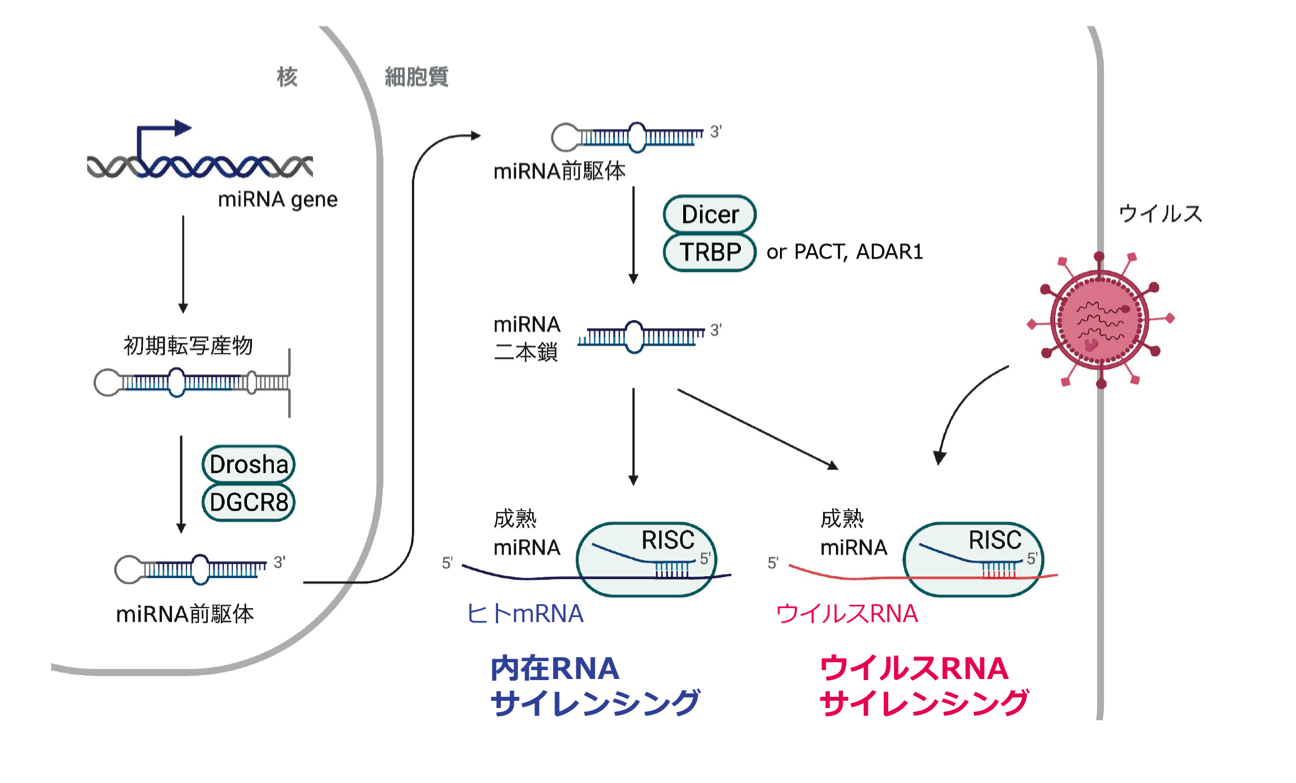 マイクロRNAは、ウイルス感染から直接、または間接的に、生体を防御している
マイクロRNAは、ウイルス感染から直接、または間接的に、生体を防御しているマイクロRNAが多様な免疫応答を制御する仕組みを探究する
まずはヒト細胞にウイルスが感染した際、マイクロRNAがどのように応答するのか、またその結果としてウイルス増殖、IFN産出、細胞死の誘導が制御されるのかを実験で検証しました。使用したのは、ヒト培養細胞と、IFNを産出し細胞死を誘導するセンダイウイルス(SeV)、IFN産出も細胞死も誘導しないボルナ病ウイルス(BoDV)です。
SeVに感染させたヒト細胞では、miR-106bという細胞死を抑制する特定のマイクロRNAの量が減少し、IFN-βとウイルスRNA量が増加、ほぼ同時にピークを迎え、その後は減少し、細胞死が誘導されました。
BoDVの感染では、miR-106bは逆に増加しました。IFN-βの発現誘導はなく、ウイルスRNAは徐々に増加し、感染3日後から急増しましたが、細胞は無症状でした。SeV感染細胞において、miR-106bを細胞内に導入することで、細胞死を抑制できることも明らかにしています。ウイルス感染により、どのようなmiRNAが、どのように発現変動し、何が起こるのかを明らかにすることで、ヒトとウイルスの多様性、また、それぞれ異なる多様な免疫応答がどのように誘導されるのかを解明したいと考えています。
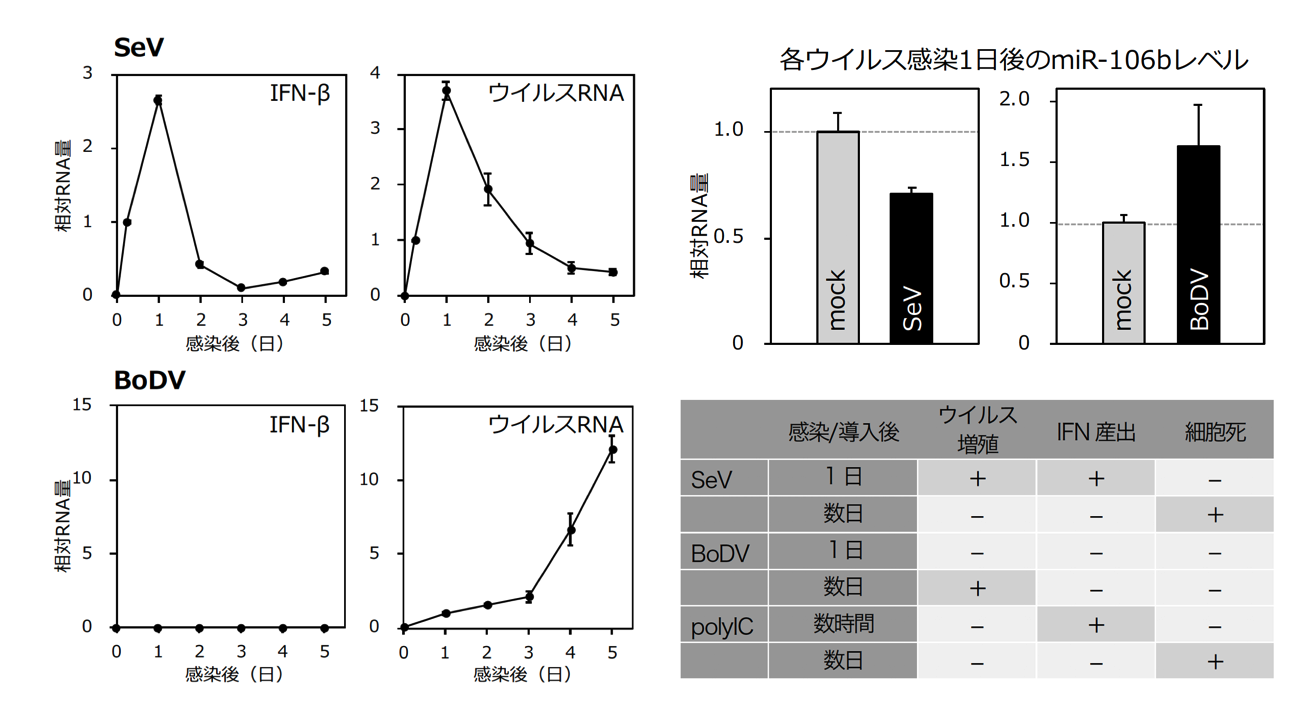 ウイルス感染後のIFN-β量、ウイルスRNA量、miR-106b量を測定
ウイルス感染後のIFN-β量、ウイルスRNA量、miR-106b量を測定